 Antes de que los intrones fueran descubiertos en 1977 por Richard Robert y Phil Sharp, se creía que el ARN mensajero era una transcripción dedicada del ADN, como lo es en muchos procariotas. Los científicos observaron por microscopía electrónica las hibridaciones del ARN transcrito con las partículas de ADN complementario (bucle R) y entendieron que las moléculas de ARNm eucariotas que alcanzaron el citoplasma son mucho más cortas que los genes con los que coinciden, lo que indica que los huecos en el ADN se eliminan. Estos se deshicieron de las partículas que se llamaron intrones. Un intrón es un tramo largo de ADN no codificante ubicado entre exones (o áreas codificantes) en una genética. La secuencia de ADN entre exones que se copia inicialmente en ARN aún se reduce de los registros de ARN finales y, por esa razón, no altera el código de aminoácidos. Se sabe que algunas series intrónicas afectan la expresión génica. Un intrón es un segmento no codificante en una longitud de ADN que altera una secuencia codificante genética o una secuencia no traducida, retirándose el segmento coincidente del duplicado de ARN antes de la transcripción. La genética que contiene intrones se conoce como genética alternativa o dividida debido al hecho de que las regiones codificantes no son continuas. Los intrones se localizan solo en microorganismos eucariotas. Un intrón es una parte de una genética que no codifica aminoácidos. Tanto en las células vegetales como en las pet, una gran cantidad de series hereditarias están divididas por uno o más intrones. Las partes de la secuencia genética que se revelan en la proteína se denominan exones debido al hecho de que son compartidas, mientras que las partes de la serie genética que no se expresan en la proteína se denominan intrones, ya que se encuentran entre los exones. El ácido desoxirribonucleico, o ADN, consiste en la base del código genético.
Antes de que los intrones fueran descubiertos en 1977 por Richard Robert y Phil Sharp, se creía que el ARN mensajero era una transcripción dedicada del ADN, como lo es en muchos procariotas. Los científicos observaron por microscopía electrónica las hibridaciones del ARN transcrito con las partículas de ADN complementario (bucle R) y entendieron que las moléculas de ARNm eucariotas que alcanzaron el citoplasma son mucho más cortas que los genes con los que coinciden, lo que indica que los huecos en el ADN se eliminan. Estos se deshicieron de las partículas que se llamaron intrones. Un intrón es un tramo largo de ADN no codificante ubicado entre exones (o áreas codificantes) en una genética. La secuencia de ADN entre exones que se copia inicialmente en ARN aún se reduce de los registros de ARN finales y, por esa razón, no altera el código de aminoácidos. Se sabe que algunas series intrónicas afectan la expresión génica. Un intrón es un segmento no codificante en una longitud de ADN que altera una secuencia codificante genética o una secuencia no traducida, retirándose el segmento coincidente del duplicado de ARN antes de la transcripción. La genética que contiene intrones se conoce como genética alternativa o dividida debido al hecho de que las regiones codificantes no son continuas. Los intrones se localizan solo en microorganismos eucariotas. Un intrón es una parte de una genética que no codifica aminoácidos. Tanto en las células vegetales como en las pet, una gran cantidad de series hereditarias están divididas por uno o más intrones. Las partes de la secuencia genética que se revelan en la proteína se denominan exones debido al hecho de que son compartidas, mientras que las partes de la serie genética que no se expresan en la proteína se denominan intrones, ya que se encuentran entre los exones. El ácido desoxirribonucleico, o ADN, consiste en la base del código genético.
Categoría de Intrones
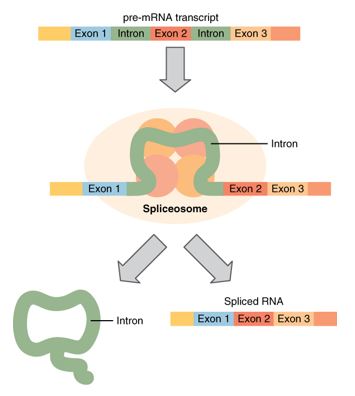 Los intrones actualmente tienen algunas categorías. Pueden ser intrones espliceosómicos, auto-empalme del Equipo I y II, o ARN de transferencia. Los intrones espliceosómicos se descubren justo en el núcleo de los genomas eucariotas y también se eliminan mediante corte y empalme. Los espliceosomas tienen una región que reconoce intrones y, con la ayuda de pequeñas ribonucleoproteínas nucleares (snRNP), inician su seno eliminando intrones y permitiendo que se desarrolle ARN mensajero completamente desarrollado con solo exones. Algunas partículas de intrones tienen la capacidad de ejecutar su propio mecanismo de escisión, sin la ayuda de los espliceosomas, llamado autoempalme. En ambas situaciones, las series intrónicas tienen la capacidad de retirarse y registrarse con los exones, sin embargo, hay una separación de grupos. El equipo I fue el primero que se encontró y también incluye un cofactor de guanina que ayuda en los procedimientos de transesterificación y unión de exones. En el Equipo II, que se encuentra en los genes mitocondriales, hay una escisión comparable a los intrones espliceosómicos, pero con un grupo hidroxilo que actúa sobre el asalto nucleófilo que permite el desarrollo de un intrón de bucle. Los intrones de ARN de transferencia (ARNt), a su vez, interrumpen las funciones estructurales vitales de la partícula de ARNt madura y pueden influir directamente en la traducción. El corte y empalme de intrones de ARNT se realiza mediante una instalación de proteínas sanas, endonucleasas que escinden el intrón y ligasas que reensamblan los exones.
Los intrones actualmente tienen algunas categorías. Pueden ser intrones espliceosómicos, auto-empalme del Equipo I y II, o ARN de transferencia. Los intrones espliceosómicos se descubren justo en el núcleo de los genomas eucariotas y también se eliminan mediante corte y empalme. Los espliceosomas tienen una región que reconoce intrones y, con la ayuda de pequeñas ribonucleoproteínas nucleares (snRNP), inician su seno eliminando intrones y permitiendo que se desarrolle ARN mensajero completamente desarrollado con solo exones. Algunas partículas de intrones tienen la capacidad de ejecutar su propio mecanismo de escisión, sin la ayuda de los espliceosomas, llamado autoempalme. En ambas situaciones, las series intrónicas tienen la capacidad de retirarse y registrarse con los exones, sin embargo, hay una separación de grupos. El equipo I fue el primero que se encontró y también incluye un cofactor de guanina que ayuda en los procedimientos de transesterificación y unión de exones. En el Equipo II, que se encuentra en los genes mitocondriales, hay una escisión comparable a los intrones espliceosómicos, pero con un grupo hidroxilo que actúa sobre el asalto nucleófilo que permite el desarrollo de un intrón de bucle. Los intrones de ARN de transferencia (ARNt), a su vez, interrumpen las funciones estructurales vitales de la partícula de ARNt madura y pueden influir directamente en la traducción. El corte y empalme de intrones de ARNT se realiza mediante una instalación de proteínas sanas, endonucleasas que escinden el intrón y ligasas que reensamblan los exones.
Función de Intrón
 Los genes son secciones de ADN que inscriben ciertos atributos de un organismo. No todas las partes de la genética son realmente componentes del código genético. Hay secciones de ADN que no codifican nada, que se llaman intrones. El código genético de un microorganismo se determina por la secuencia de nucleótidos que componen su ADN. Los tripletes de nucleótidos codifican aminoácidos específicos, que son los componentes básicos de las proteínas saludables. La secuencia de aminoácidos determina qué proteína debe crearse dentro de una célula.
Los genes son secciones de ADN que inscriben ciertos atributos de un organismo. No todas las partes de la genética son realmente componentes del código genético. Hay secciones de ADN que no codifican nada, que se llaman intrones. El código genético de un microorganismo se determina por la secuencia de nucleótidos que componen su ADN. Los tripletes de nucleótidos codifican aminoácidos específicos, que son los componentes básicos de las proteínas saludables. La secuencia de aminoácidos determina qué proteína debe crearse dentro de una célula.
Esto, en consecuencia, determina el marco y también la función de la célula. Para que se cree una proteína a partir de ADN, se llevan a cabo 2 procedimientos. Primero, toda la cadena de ADN se transcribe directamente en ARN mensajero o ARNm. Ahora, los intrones, o componentes innecesarios de la molécula de ADN, consisten en la molécula de ARNm, que se denomina transcripción primaria. Actualmente, los intrones ya tienen algunas funciones definidas. Participan de forma proactiva en el control de la expresión génica, por ejemplo, con corte y empalme alternativo. En él, se hacen combinaciones de diferentes exones en la transcripción clave, creando más de una proteína saludable con un solo gen. Asimismo, pertenece al „barajado de exones”, un procedimiento que permite la formación de nuevos genes. En él, tiene lugar una recombinación de partículas de ADN que permite colocar exones en varias ubicaciones y también, de esta manera, se producen nuevas series. Con las bases de datos de secuenciación, se determinó que los intrones se distribuyen de forma conservada en el genoma de organismos eucariotas de diferente complejidad. Por lo tanto, se cree que en el avance de la fabricación de proteínas saludables en las instalaciones, los dominios se barajaron y también se recolectaron con el fin de producir series completamente nuevas para la formación de proteínas saludables con diferentes características. En conjunto, hay pocos registros de secuencias intrónicas en procariotas, sin embargo, una gran parte del genoma de los eucariotas está formado por ellas. Los primates tienen un grosor alto, mientras que los seres vivos mucho menos intrincados tienen una cantidad menor. Su tamaño también difiere, siendo varios también dentro de los mismos tipos. Los intrones tienen diferentes dimensiones y se cree que esto está directamente relacionado con la expresión genética, ya que en realidad se ha observado que en muchos organismos, cuando los intrones son más pequeños, los genes tienden a revelarse más. Los intrones también se pueden utilizar como plumas genéticas polimórficas, el más utilizado es el polimorfismo de tamaño de intrón/ ILP. Por lo general, se utiliza en estudios de población, ya que se determina convenientemente en estrategias moleculares. A través de PCR (Reacción en Cadena de la Polimerasa) es posible encontrar modificaciones en la serie variable de intrones que están flanqueados por exones muy conservados.
